Halogenação
Nitração e sulfonação
Alquilação e acilação de Fridel-Crafts
Saponificação e transesterificação
Processo de Kolbe e Dumas
Sintese de Wurtz e Willanson
Reações de Substituição
Falando de uma forma genérica, as reações de substituição são aquelas em que SUBSTITUÍMOS um hidrogênio de um composto orgânico por algum grupo de outro reagente, que em alguns casos será inorgânico e em outros casos, orgânico.
Isso ocorre quando colocamos o substrato (composto orgânico que terá um de seus H substituído) em contato com o reagente, em presença ou não de catalisador (a depender dos reagentes utilizados), e resulta em 2 outros compostos, funcionando de maneira análoga às reações de DUPLA-TROCA ou DESLOCAMENTO, que aprendemos na química inorgânica.
Veja o caso geral abaixo, em que o substrato é o metano e o reagente é um composto hipotético XY:
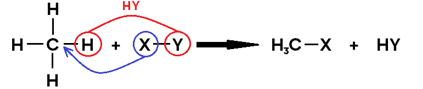
Obs.: As reações de substituição nos hidrocarbonetos são típicas de hidrocarbonetos saturados (alcanos e ciclanos), mas também pode ocorrer no benzeno. Neste material, no entanto, não abordaremos estes aromáticos ainda.
Halogenação
· Ocorre com adição de HALOGÊNIOS (Cl2 ou Br2, uma vez que o F2 é reativo demais, sendo até explosivo, e o I2 tem reação lenta demais) aos alcanos e ciclanos;
· O hidrogênio é substituído por um dos átomos do halogênio molecular;
· Utiliza LUZ (λ) E CALOR (Δ) como catalisadores;
· Em alcano, os produtos formados são um HALETO DE ALQUILA e um HIDRÁCIDO HALOGENADO;
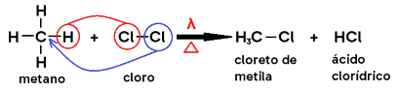
Importante à beça:
Ao fazermos a cloração do metilbutano, encontram-se os seguintes produtos com suas proporções:
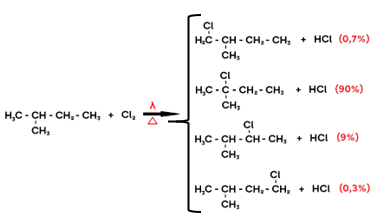
Como 90% dos produtos formados foram com substituição em hidrogênio terciário, 9% em hidrogênio secundário e 1% em hidrogênio primário, conclui-se que a ORDEM DE REATIVIDADE DO HIDROGÊNIO é a seguinte:
H terciário > H secundário > H primário
Sendo assim, o PRODUTO PRINCIPAL de uma substituição em alcano será aquele em que o grupo substituinte se ligou ao CARBONO MENOS HIDROGENADO.
· Em cicloalcano, os produtos formados são um HALETO DE CICLOALQUILA e um HIDRÁCIDO HALOGENADO;
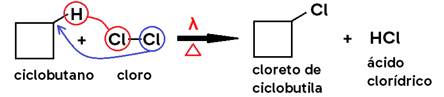
Obs.:
a. Lembrando que caso o catalisador, em vez de luz e calor, fosse um ácido de Lewis, a reação seria a de adição, e não substituição, como já vimos;
b. No ciclopropano, não ocorre a reação de substituição, mesmo em presença de luz e calor;
c. No ciclopentano e no ciclohexano, não ocorre reação de adição, mesmo em presença de ácido de Lewis, devido à pouca tensão em seus aneis.