Oxidação branda de alceno
Oxidação enérgica de alceno
Ozonólise
Oxidação de Alcinos e ciclanos
Oxidação de álcoois
Reação de eliminação
Regra de Saytzef
Desidratação intramolecular e intermolecular
I - Reação de oxidação
Oxidação em Alcenos (ligações duplas)
a) Oxidação branda
É feita oxidante em uma solução aquosa diluída, neutra ou levemente alcalina, geralmente, de permanganato de potássio. Indicamos o agente oxidante por [O] e temos a formação de um diálcool, também chamado de diol ou glicol:
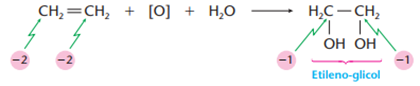
Ricardo Feltre, volume único, 6ª ed, 2004.
Obs.: Reparem no aumento do nox do carbono, ou seja, perda de elétrons, caracterizando uma oxidação.
b) Oxidação enérgica
É feita usando-se como oxidante, uma solução aquosa de permanganato ou dicromato de potássio em meio ácido(em geral H2SO4).
O agente oxidante formado atacará o alceno, quebrando a molécula na ligação dupla e produzindo ácido carboxílico e/ou cetona e/ou gás carbônico (CO2 ):
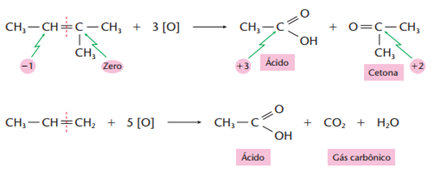
Ricardo Feltre, volume único, 6ª ed, 2004.
O tipo de produto obtido depende da posição da ligação dupla:
• Se • carbono for primário produz CO2 e H2O;
• Se • carbono for secundário produz ácido carboxílico;
• Se • carbono for terciário produz cetona.
c) Ozonólise
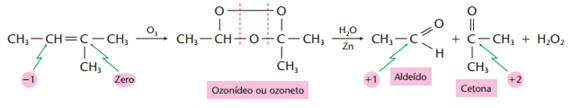
Ricardo Feltre, volume único, 6ª ed, 2004.
Aqui, o zinco é utilizado para quebra da água oxigenada (H_2O_2H2O2), impedindo que ela oxide o aldeído para ácido carboxílico.
Podemos perceber que:
• O carbono primário ou secundário da ligação dupla produz aldeídos;
• O carbono terciário produz cetona.
Oxidação em Alcinos (ligações triplas)
a) Oxidação branda
Utilizando o permanganato de potássio (KMnO_4KMnO4) em solução aquosa neutra ou levemente alcalina, os alcinos produzem dicetonas, compostos orgânicos com duas carbonilas secundárias:
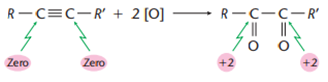
Ricardo Feltre, volume único, 6ª ed, 2004.
Obs.: Caso R ou R’ for o hidrogênio, nessa extremidade, ocorrerá formação de um aldeído.
b) Oxidação enérgica
Essa oxidação é feita com aquecimento, de solução ácida de permanganato de potássio(KMnO4). Há quebra da cadeia por completo, diferente da oxidação branda, onde somente as ligações Pi(π) são quebradas, e por fim, forma-se ácidos carboxílicos.
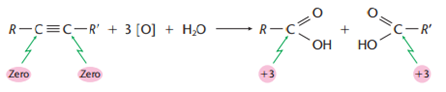
Ricardo Feltre, volume único, 6ª ed, 2004.
Obs.: Caso R ou R’ for o hidrogênio, ao invés da formação dos ácidos, teremos CO2 e H2O.
Oxidação de ciclanos
A teoria das tensões dos anéis de Baeyer diz, resumidamente, que:
“Nos ciclanos, as valências devem ser entortadas ou flexionadas para fechar o anel, e isso cria uma tensão que torna o anel instável (ou seja, de fácil ruptura).”
Anéis de 3 e 4 carbonos são quebrados com maior facilidade por conta dessa tensão. Oxidantes mais fortes como HNO3 concentrado, KMnO4 em solução ácida, conseguem quebrar também os anéis de 5 e 6 carbonos. Na quebra desses anéis, são produzidos ácidos dicarboxílicos (diácidos):
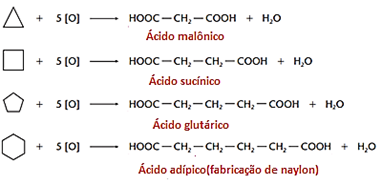
Obs.: Uma importante diferenciação em relação aos alcenos, é que o KMnO4, em solução aquosa neutra, não reage com os ciclanos.
Oxidação de álcoois
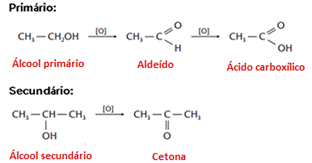
Os oxidantes enérgicos, como KMnO4 ou K2Cr2O7 em meio ácido, serão usados na oxidação de álcoois, e seus produtos se diferenciam pelo tipo de álcool que será oxidado: Primário, secundário ou terciário.
Obs.: Álcoois terciários não se oxidam, caso as condições de oxidação sejam extremas, a molécula irá quebra-se.
Combustão
Em geral, os compostos orgânicos sofrem combustão. Essa reação é uma oxidação acontece com o rompimento da cadeia carbônica, liberando grande quantidade de energia e gerando como produto COCO(se a reação for incompleta) ou CO_2CO2(se a reação for completa). O hidrogênio produz H_2OH2O, o nitrogênio produz NONO ou NO_2NO2 ; e assim por diante.
Veja os exemplos:
Combustão completa

Combustão incompleta

O éter mais comum, o dietílico, é muito inflamável e até explosivo. Sua combustão completa segue o padrão de combustão e tem com produtos os mesmos das combustões orgânicas: CO_2CO2 e H_2OH2O.
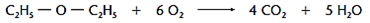
Obs.: Os éteres (especialmente o éter dietílico) quando oxidados lentamente pelo oxigênio do ar, dão origem a peróxidos:
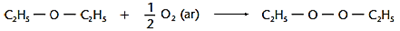
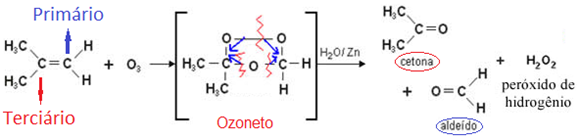
Ozonólise
• Ocorre em alcenos;
• Emprega-se como agente oxidante o ozônio (O3);
• Há a reação do alceno com água;
• Utiliza zinco (Zn) como catalisador;
• A ligação dupla é rompida e os oxigênios do ozônio se ligam aos carbonos da dupla, formando um composto intermediário instável chamado ozoneto;
• Depois, as ligações envolvidas com os oxigênios se quebram, liberando um oxigênio que oxida a água do meio, formando água oxigenada (H2O2);
• Forma-se, também, um aldeído, caso o carbono da dupla seja primário ou secundário; e/ou uma cetona, caso o carbono da dupla seja terciário.
II - Reação de eliminação
Reações de eliminação nada mais são, reações que acontecem saída de dois átomos ou grupos vizinhos com a formação de uma ligação dupla ou ciclização da cadeia em casos mais raros. Basicamente, existem quatro tipos de reação de eliminação:
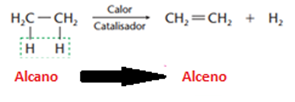
a) Eliminação de hidrogênio (desidrogenação)
A partir dos alcanos (existentes em grande quantidade no petróleo) obtemos alcenos, por isso essa reação é de grande importância na indústria petroquímica.
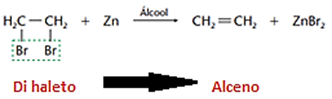
b) Eliminação de halogênios (de-halogenação)
Na eliminação de halogênios, que são eletronegativos, usamos um metal por ser eletropositivo (geralmente Zinco), catalisado por um álcool
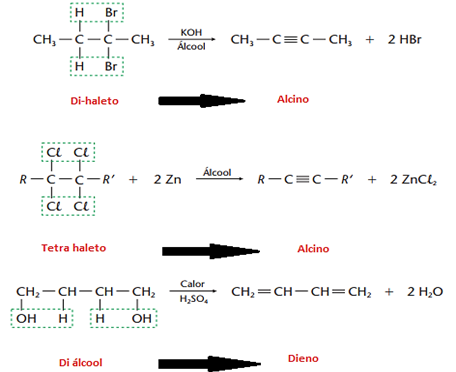
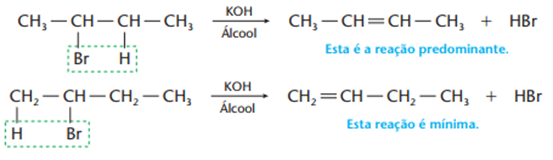
c) Eliminação de halogenidretos, HCl, HBr, HI (desidro-halogenação)
Esse tipo de reação é obtida por meio de KOH em dissolvida em álcool, e faz sentido, pois éinteressante usar uma base (KOH) para arrancar um ácido (HCl, HBr, HI…) de uma molécula orgânica. Se seu reagente for um haleto de cadeias maiores, haverá maior tendência de o hidrogênio sair do carbono menos hidrogenado. Esta é a regra de Saytzef, que basicamente é o inverso da regra de Markownikoff. Temos duas possibilidades para, por exemplo, o 2–bromo-butano, veja:
Ricardo Feltre, volume único, 6ª ed, 2004.
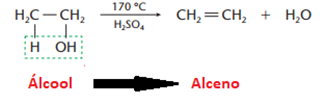
d) Eliminação de água (desidratação)
• Desidatração intramolecular (ocorre na própria molécula de álcool)
• Desidatração intermolecular (ocorre entre duas moléculas de álcoois iguais ou diferentes, com formação de éter)

Se o reagente for um álcool de cadeia maior, haverá também obediência à regra de Saytzef, como vemos no exemplo abaixo:
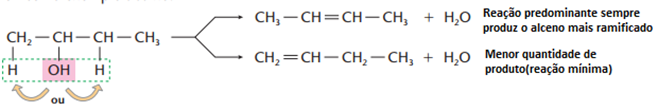
Ricardo Feltre, volume único, 6ª ed, 2004.
Obs.: Essa reação é comum para álcoois primários. Álcoois secundários e principalmente terciários tendem a desidratar-se intramolecularmente, tendo como produto, os alcenos correspondentes.
• Desidratação de ácidos carboxílicos
Aqui, há formação do anidrido do ácido correspondente:
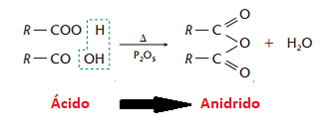
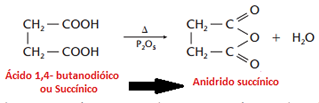
Os anidridos cíclicos mais estáveis são aqueles com 5 e 6 átomos de carbono, de acordo com a teoria das tensões de Baeyer:
Obs.: Apenas o ácido fórmico não dá anidrido
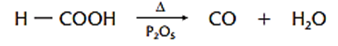
Eliminações Múltiplas ou sequenciais
Pode ocorrer reações de eliminação duas vezes na mesma molécula, assim, teremos a formação de uma ligação tripla ou de duas ligações duplas, como vemos abaixo: