Oxidação de Alcenos
Ozonólise
Oxidação de Alcinos
Oxidação de Álcool Primário
Oxidação de Álcool Secundário
Questão sobre Oxidação
Questão sobre Oxidação Enérgica
Reações de Oxidação
Oxidação em Alcenos (ligações duplas)
Oxidação branda
É feita oxidante em uma solução aquosa diluída, neutra ou levemente alcalina, geralmente, de permanganato de potássio. Indicamos o agente oxidante por [O] e temos a formação de um diálcool, também chamado de diol ou glicol:
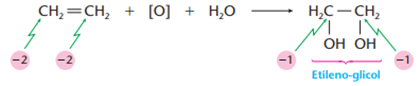
Obs.: Reparem no aumento do nox do carbono, ou seja, perda de elétrons, caracterizando uma oxidação.
Oxidação enérgica
É feita usando-se como oxidante, uma solução aquosa de permanganato ou dicromato de potássio em meio ácido (em geral H2SO4).
O agente oxidante formado atacará o alceno, quebrando a molécula na ligação dupla e produzindo ácido carboxílico e/ou cetona e/ou gás carbônico (CO2):
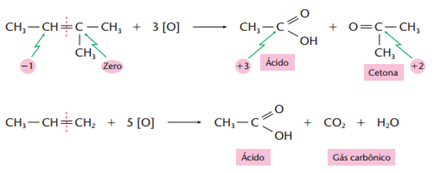
O tipo de produto obtido depende da posição da ligação dupla:
· Se • carbono for primário produz CO2 e H2O;
· Se • carbono for secundário produz ácido carboxílico;
· Se • carbono for terciário produz cetona.
Ozonólise
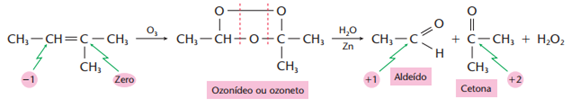
Aqui, o zinco é utilizado para quebra da água oxigenada (H2O2), impedindo que ela oxide o aldeído para ácido carboxílico.
Podemos perceber que:
· O carbono primário ou secundário da ligação dupla produz aldeídos;
· O carbono terciário produz cetona.
Oxidação em Alcinos (ligações triplas)
Oxidação branda
Utilizando o permanganato de potássio (KMnO4) em solução aquosa neutra ou levemente alcalina, os alcinos produzem dicetonas, compostos orgânicos com duas carbonilas secundárias:
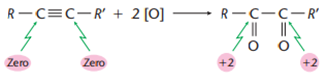
Obs.: Caso R ou R’ for o hidrogênio, nessa extremidade, ocorrerá formação de um aldeído.
Oxidação enérgica
Essa oxidação é feita com aquecimento, de solução ácida de permanganato de potássio(KMnO4). Há quebra da cadeia por completo, diferente da oxidação branda, onde somente as ligações Pi(π) são quebradas, e por fim, forma-se ácidos carboxílicos.
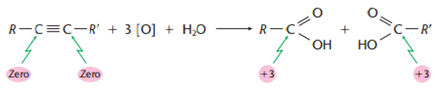
Obs.: Caso R ou R’ for o hidrogênio, ao invés da formação dos ácidos, teremos CO2 e H2O.