As variáveis de estado
A transformação isotérmica
A transformação isovolumétrica
A transformação isobárica
Exercício 5 de aula sobre equação geral dos gases
Variáveis de estado
Quando vamos falar sobre o estado gasoso nós precisamos compreender as três variáveis de estado: pressão, volume e temperatura. Elas estão relacionadas com as propriedades e características dos gases.
Pressão
Nos gases a pressão será gerada pelos choques das partículas do gás nas paredes do recipiente. Como essas partículas estão em movimento, elas se chocam contra as paredes.
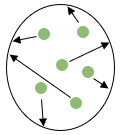
Nós podemos pensar então que quanto mais partículas de gases por uma certa área nós tivermos ali dentro, maior será a pressão.
Pressão atmosférica
É a pressão que os gases atmosféricos causam sobre a superfície terrestre. Ao nível do mar, essa pressão é de 1 atm, que pode ser expressa em mmHg.
1 atm = 760 mmHg
A pressão atmosférica pode variar de acordo com a altitude. Isso ocorre porque regiões mais altas, a quantidade de partículas sobre uma determinada area é menor.
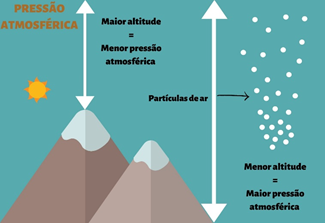
Volume
Um gás ocupa o volume do recipiente em que ele está contido. Se nós estamos com um certo gás contido numa garrafa, caso a gente abra ele numa sala, o volume ocupado passa a ser o da sala.
Unidades de volume
1 m3 = 1000 L
1 dm3 = 1 L
1 cm3 = 1 mL
Temperatura
Essa variável está relacionada com o grau de agitação das moléculas. Quanto maior foi a agitação das moléculas, maior será a temperatura. Podemos falar que em temperaturas maiores a energia cinética média das partículas são maiores.
Unidades de temperatura
Celsius (°C) e Kelvin (K)
27 °C = 300 K
0 °C = 273 K
Já sabendo das três variáveis de estado. Nós podemos submeter os gases a certas transformações. Alterando essas variáveis. Elas podem ser de três tipos: Isobárica, Isovolumétrica ou isotérmica.
OBS: Essas transformações são para gases ideias com quantidades iguais. Não podemos alterar o número de mols, se não as relações darão errado.
Isotérmica
Nessa transformação a temperatura permanece constante. Essas transformação foi estuda pelo químico Robert Boyler que deu origem a Lei de Boyle. Essa lei propõe a seguinte fórmula:
(P.V)antes = (P.V)depois
Numa transformação isotérmica, nós podemos dizer que ao aumentarmos a pressão, o volume diminui. Esse produto P.V é sempre constante.
Graficamente:
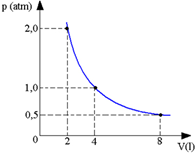
Isovolumétrica
Nessa transformação o volume permanece constante. Essa transformação é expressa pela segunda lei de Charles e Gay-Lussac, que diz que se aumentarmos a temperatura de um sistema, a pressão exercida pelo gás também aumenta, ou seja, diretamente proporcionais. Teremos então a seguinte fórmula:
(P/T)antes = (P/T)depois
OBS: Temperatura em Kelvin (K).
Graficamente
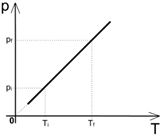
Isobárica
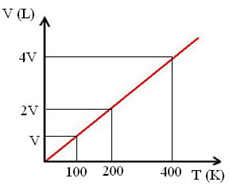
Nessa transformação a pressão é constante. Também é uma lei de Charles e Gay-Lussac, porém essa é a primeira lei de Charles e Gay-Lussac. Diz que se a pressão é mantida constante, o volume do gás é diretamente proporcional a sua temperatura. Ou seja, se aumentarmos o volume, a temperatura também irá aumentar.
(V/T)antes = (V/T)depois
Graficamente:
Equação geral dos gases
Juntando todas as reações numa só, nós chegamos na equação geral dos gases. Essa aequação só é válida para uma transformação que possui e mesma quantidade de matéria antes e depois da transformação. Lembre-se que a temperatura é sempre em kelvin.
