Equilíbrio Químico de uma Reação Qualquer
Equilíbrio Químico Utilizando Estequiometria
Cálculo das Constantes de Equilíbrio Kc e Kp
Equilíbrio Químico Considerando Dissociação Parcial
Cálculo da Concentração dos Reagentes no Equilíbrio
Fatores que Alteram o Equilíbrio Químico
Equilíbrio químico
Existem reações onde os reagentes e os produtos estão em constante reação em processos opostos, tais reação chamamos de reações reversíveis, que quando com a mesma velocidade de reação em ambos os sentidos atingem o equilíbrio químico.
Exemplo:
N2 (g) + 3 H2(g) ⇌ 2 NH3(g)
A reação representada acima de produção da amônia (NH3) é uma reação reversível, onde a todo momento temos H2 e N2 reagindo para formar NH_33, mas também temos a amônia (NH3) se decompondo e voltando a se tornar H2 e N2. Quando estas velocidades de reação em ambos os sentidos se igualam, dizemos que alcançamos o equilíbrio químico.
Gráfico de equilíbrio químico
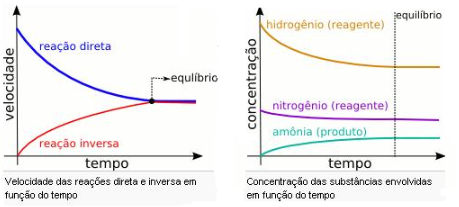
PSIU!!
No momento em que as velocidades ou concentração se tornam constantes atingimos o equilíbrio químico da reação.
Expressão para equilíbrio químico e a constante kc
Em 1886, químicos noruegueses descobriram existir uma relação entre a concentração dos reagentes e dos produtos em equilíbrio químico, excluindo os reagentes e produtos no estado físico sólido. Essa relação foi chamada de Lei de Ação das massas, onde para uma reação reversível genérica:
aA + bB ⇌ cC + dD
Temos que a relação entre as concentrações será:
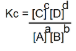
Onde Kc é a nossa constante de equilíbrio.
PSIU!!
Quanto maior o valor de Kc, maior a tendência de ocorrer a reação no sentido de formação dos produtos.
Quanto menor o valor de Kc, maior a tendência de ocorrer a reação no sentido de formação dos reagentes.
PSIU 2!!
Em soluções aquosas, a concentração da água deve ser considerada constante, é não aparecerá na expressão do Kc e sólidos nunca participaram do cálculo do Kc.
Expressão para equilíbrio químico e a constante kp
Com relação aos gases participantes do equilíbrio, podemos gerar uma relação entre reagentes e produtos através de suas pressões parciais, já que essas pressões são proporcionais as suas molaridades.
Exemplo:
Para a reação: aA + bB ⇌ cC + dD
Temos que a relação entre as pressões parciais será:
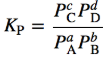
Onde Kp é a nossa constante de equilíbrio em relação a pressão parcial.
PSIU!!
Para cálculo de Kp não apareceram na expressão substâncias nos estados físicos sólidos e líquidos.
Relação entre Kp e Kc
É possível chegar a uma relação entre Kc e Kp através da equação:
Kp = Kc . (R . T)^(∆n)