Bases ou hidróxidos
Nomenclatura das Bases
Classificação das Bases
Bases no dia a dia
Questão sobre Óxidos Básicos
Questão sobre NaOH
Segundo Arrhenius, são substâncias inorgânicas que quando colocadas em presença de água sofrem dissociação iônica, liberando como único ânion a hidroxila (OH-).
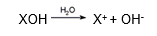
Classificação
Quanto ao número de hidroxilas
Em função do número de hidroxilas(OH-) liberadas quando sofrem dissociação iônica, uma base pode ser classificada como:

Quanto à solubilidade em água
Solubilidade de uma base é a propriedade que indica o quanto uma base é capaz de se dissolver em água, ela pode ser classificada como:
• Solúvel: Possui grande capacidade de se dissolver em água. São as bases formadas por elementos da família IA e NH_4^+4+.
• Parcialmente solúvel: Pouco capaz de se dissolver em água. São as bases formadas por elementos da família IIA.
• Insolúvel: Não é capaz de se dissolver em água. São as bases formadas pelos demais elementos.
Quanto a força
A força de uma base é dada pela sua capacidade de liberar OH- (sofrer dissociação iônica) quando colocadas em presença de água, quanto maior a quantidade de OH- liberados, maior será a força da base.
• Forte: São as bases formadas por elementos do grupo 1 e 2
• Fraca: São as bases formadas pelos demais elementos.
Importante: As bases formadas por Mg(OH)2 e Be(OH)2, que são elementos do grupo 2, são consideradas insolúveis e fracas.
Nomenclatura
Elementos com NOX fixo:
Família IA, IIA, Ag+1, Zn+2, Cd+2, Al+3 e NH4 +1.
Hidróxido de nome do elemento
Ex.: NaOH - Hidróxido de sódio
Mg(OH)2 - Hidróxido de magnésio
Al(OH)3 - Hidróxido de alumínio
Elementos com NOX variável:
Fe, Co, Ni = +2 ou +3
Cu, Hg = +1 ou +2
Au = +1 ou +3
Pb, Pt, Sn = +2 ou +4
Hidróxido de nome do elemento + NOX(em romanos) ou Hidróxido de nome do elemento + sufixo OSO (menor NOX) / sufixo ICO (maior NOX)
Ex.: CuOH - Cu com nox +1 - Hidróxido de cobre I ou Hidróxido cuproso
Cu(OH)2 - Cu com nox +2 - Hidróxido de cobre II ou Hidróxido cúprico
Pb(OH)2 - Pb com nox +2 - Hidróxido de chumbo II ou Hidróxido plumboso
Pb(OH)4 - Pb com nox +4 - Hidróxido de chumbo IV ou Hidróxido plúmbico
Formulação das bases
Quando precisamos montar a fórmula de uma base a partir de seu nome, basta unir o cátion desejado ao ânion OH- . Note que a carga total do OH- deverá anular a carga total do cátion.
Ex.: Hidróxido de cálcio
Ca+2 e OH−
logo para anular a carga +2 do cálcio precisamos de 2 ânions OH−
Ca+2 + 2OH− → Ca(OH)2
Hidróxido férrico
Fe+3 e OH−
logo para anular a carga +3 do ferro precisamos de 3 ânions OH-
Fe+3 + 3OH− → Fe(OH)3