Introdução
Propriedades gerais da matéria
Propriedades específicas da matéria
Estados físicos e mudanças de estados físicos da matéria
Divisão da matéria (substâncias puras e misturas)
Exercício de propriedades da matéria
Exercício sobre misturas homogêneas e heterogêneas
A Química é a ciência que estuda a constituição da matéria, que nada mais é que tudo aquilo que possui massa e ocupa lugar no espaço, sua estrutura interna e as relações entre os diversos tipos de materiais encontrados na natureza, além de determinar suas propriedades, sejam elas físicas como por exemplo, cor, ponto de fusão, densidade e etc, ou químicas, que são as transformações de uma substância em outra.
Matéria se define como qualquer coisa ou substância que apresente massa e ocupe lugar no espaço (apresente volume). Água, madeira, vidro, ar, alumínio, são exemplos de matéria. Frequentemente fala-se de matéria de forma mais específica: corpos ou objetos.
Chamamos de corpo qualquer porção limitada de matéria. Um pedaço de madeira ou um caco de vidro são exemplos de corpo.
Objetos são corpos que servem a uma determinada função. Por exemplo, cadeira de madeira, copo de vidro, panela de aço.
Propriedades específicas da matéria
Propriedades Gerais da matéria
São as características que toda matéria apresenta, independentemente do seu estado físico.
- Inércia: Uma matéria sempre apresenta a tendência de manter o seu estado, seja de repouso, seja de movimento.
- Massa: Fisicamente, massa é uma grandeza que indica a medida da inércia ou da resistência de um corpo de ter seu movimento acelerado. Porém, podemos, de uma forma geral, associar a massa à quantidade de partículas existentes em uma matéria.
- Volume: É o espaço que uma matéria ocupa.
- Impenetrabilidade: Duas matérias não podem ocupar o mesmo espaço ao mesmo tempo.
- Compressibilidade: É a característica que a matéria apresenta de diminuir o espaço que estava ocupando quando submetida a uma força externa.
- Elasticidade: É a característica que uma matéria tem de voltar à sua forma original quando uma força externa a estica ou comprime.
- Divisibilidade: É a capacidade que a matéria possui de ser dividida inúmeras vezes sem deixar de ser o que ela é.
Propriedades físicas
- Ponto de Fusão (PF): É a temperatura em que ocorre a passagem do estado sólido para o líquido a uma determinada pressão.
- Ponto de Ebulição (PE): É a temperatura em que ocorre a passagem do estado líquido para o gasoso a uma determinada pressão.
- Densidade: É a relação entre a quantidade de matéria em massa e o seu volume. A densidade absoluta de um corpo é igual a m/V. Se a massa é medida em gramas e o volume em centímetros cúbicos, a densidade é obtida em gramas por centímetros cúbicos.
- Solubilidade: É a característica que uma determinada matéria apresenta de dissolver outra. Por exemplo, a solubilidade do salde coisinha em água é encontrada pela relação da quantidade de sal que é solubilizado em determinada quantidade de água.
- Dureza: É a capacidade que um material tem de riscar outro. Por exemplo, o diamante é considerado o material com maior dureza conhecida, pois ele consegue risca quaisquer outros materiais.
- Tenacidade: Algumas pessoas acabam confundindo tenacidade com dureza, mas tenacidade é a capacidade que uma matéria tem de resistir ao impacto com outra matéria. Quando uma pedra é arremessada no vidro, este se quebra, ou seja, a pedra é mais tenaz que o vidro.
Propriedades Organolépticas
É a propriedade que a matéria tem de estimular pelo menos um dos nossos cinco sentidos, audição, visão, paladar, olfato e tato.
Substância x Mistura
Substância pura (ou Substância ou Espécie Química): é formada exclusivamente por partículas (moléculas ou átomos) quimicamente iguais, ou melhor, de uma única. Apresenta temperaturas de fusão e ebulição constantes.
As substâncias puras podem ser:
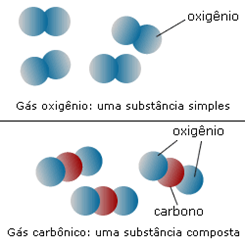
- Substância simples: formadas por átomos iguais ou átomos do mesmo elemento químico. Exemplo: o gás oxigênio (O2), que é uma substância pura simples, pois é formado apenas pelo elemento oxigênio.
- Substância compostas: formadas por átomos diferentes ou átomos de diferentes elementos químicos. Exemplo: água (H2O), que é uma substância pura composta, pois contém dois elementos em suas moléculas que são o hidrogênio e o oxigênio.
Mistura: é a reunião de duas ou mais substâncias sem que haja reação química entre elas, e mantendo cada qual suas propriedades. Apresenta temperaturas de fusão e/ou ebulição variáveis. As misturas podem ser classificadas em:
- Mistura homogênea: apresentam uma única fase, ou seja, monofásica. Exemplo: sal + água; açúcar + água; álcool + água.
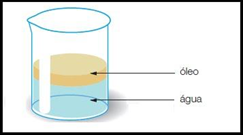
- Mistura heterogêneas: podem apresentar duas ou mais fases. São denominadas polifásicas. Exemplo: areia + água; óleo + água; talco + água.
- Qualquer porção do Universo submetida a análise é denominada sistema, e tudo que a rodeia é chamado de meio ambiente, esses sistemas podem ser dividi-os em:
Sistema aberto: tem a capacidade de trocar energia e matéria com o meio;
Sistema fechado: tem a capacidade de trocar somente energia com o meio;
Sistema isolado: não realiza nenhuma troca com o meio, esse tipo de sistema só existe de forma teórica.
Atenção:
Sistema homogêneo: É todo sistema que possui somente uma fase e necessariamente precisar ser uma mistura. Exemplo: cachaça, formada por água e álcool.
Sistema heterogêneo: É todo sistema que possui duas ou mais fases e não necessariamente precisa ser uma mistura. Exemplo: Água + Gelo e Água + areia.
Alotropia
É quando um mesmo elemento é capaz de formar substâncias simples diferentes, tais substâncias são denominadas alótropos ou formas alotrópicas. A alotropia por ser classificada de duas formas:
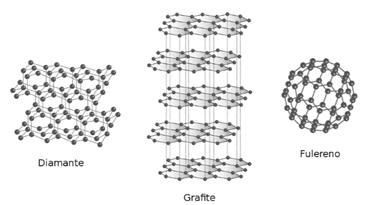
• Por estrutura: Ocorre quando um mesmo elemento é capaz de se ligar de formas diferentes, formando assim composto com propriedades distintas. Exemplo: C diamante, C grafite e C fulereno.
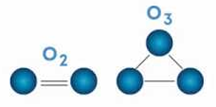
• Por atomicidade: Ocorre quando o mesmo elemento forma substâncias simples diferentes por conter diferentes quantidades de átomos na sua estrutura. Exemplo: O2 – Gás oxigênio; O3 – Gás oxônio
Estado físico da matéria
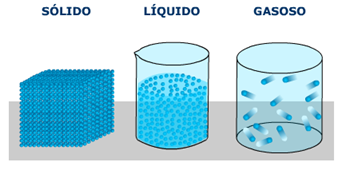
A matéria se apresenta em três estados físicos que também podem ser chamados de estados ou fases de agregação, são eles: sólido, líquido e gasoso.
Sólidos
Estado físico onde as interações intermoleculares são extremamente fortes e com isso faz com que sua forma e volume sejam fixas, ou seja, elas não se moldam ao tipo de recipiente em que se encontram. Já em relação a agitação das moléculas, os sólidos têm um grau de agitação das moléculas baixa.
Líquidos
Os líquidos têm suas interações intermoleculares com um maior comprimento que dos sólidos por exemplo, isso faz com que esse estado físico assuma uma forma fluída e se molde a forma do recipiente aonde se encontra. Por mais que sua forma tenha essa característica “moldável” seu volume é fixo, pois o seu grau de agitação ser intermediário, ou seja, maior que dos sólidos, porém menor que dos gases, ainda não é suficiente para fazer com que seu volume seja variável.
Gases
Em virtude da baixa interação entre as moléculas nesse estado físico, as partículas se movimentam espontaneamente, o grau de agitação das moléculas nos gases é elevado, e com isso vem a explicação do fato da forma e do volume dos gases serem variáveis e ocuparem todo o volume do recipiente que podem se encontrar.
Atenção! O plasma é formado por uma massa de gás ionizado em altíssima temperatura e por isso são basicamente íons e elétrons livres. O plasma possui características parecidas com a dos gases, pois também não possuem formas nem volumes fixos, porém, apresentam uma densidade muito menor.
Mudança de estado físico da matéria
É importante ressaltar que as energias desses estados são diferentes, logo as transformações feitas requerem quantidades de calor diferentes em diferentes sentidos dependendo da transformação feitas. Veja as figuras abaixo:


Importante: Nos processos endotérmicos há a absorção de calor e nos processos exotérmicos há a liberação de calor.
As passagens entre os três estados físicos (sólido, líquido e gasoso) têm o nome de mudanças de estado físico. Importante lembrar que alguns autores consideram o plasma como um quarto estado físico.
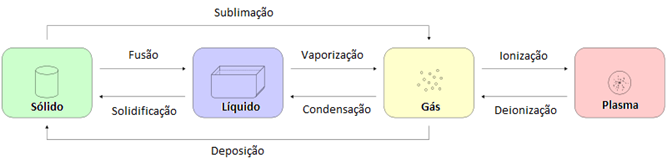
A vaporização pode ser subclassificada como:
• Evaporação: vaporização lenta, em que algumas partículas adquirem energia o bastante para se desprender da fase líquida;
• Ebulição: vaporização intermediária, em que existe equilíbrio entre fase líquida e gasosa; ocorre em uma temperatura definida para cada substância, a uma determinada pressão, chamada ponto de ebulição ou temperatura de ebulição.
• Calefação: vaporização instantânea; ocorre quando um líquido entra em contato com uma superfície sólida com temperatura mais elevada que seu ponto de ebulição.
Substâncias Puras
As transformações físicas das substâncias puras ocorrem a temperaturas constantes, como vemos a seguir:
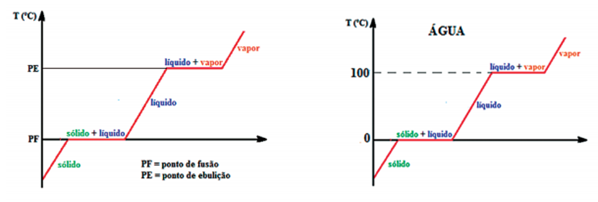
Os patamares do gráfico mostram que coexistem dois estados físicos.
Misturas
As transformações físicas das misturas não ocorrem a temperaturas constantes, como mostra o gráfico a seguir.
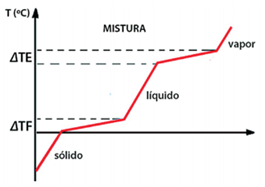
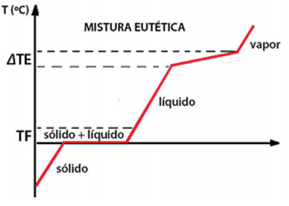
Misturas Eutéticas
Essas misturas comportam-se como se fossem substâncias puras durante sua fusão, ou seja, apresentam transformação física constante durante a sua fusão. Exemplo: solda (estanho + chumbo)
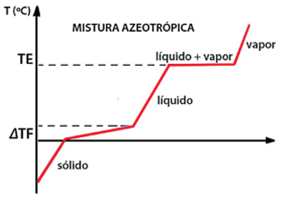
Misturas Azeotrópicas
Essas misturas comportam-se como se fossem substâncias puras durante sua ebulição, ou seja, apresentam transformação física constante durante a sua ebulição. Exemplo: solução alcoólica (96% de álcool + 4% de água).