Análise funcional da sibutramina
Análise funcional do Limoneno
Fórmula estrutural de hidrocarbonetos
Hibridação sp2 e elétrons π
Orbitais atômicos do carbono e hidrogênio
Fórmula molecular de um composto X
Ligações químicas de um alceno
Análise funcional do isoctano
Funções e nomenclatura de um alceno
Nomenclatura de um composto orgânico
O que é química orgânica?
A química orgânica é o ramo da química responsável pelo estudo dos compostos que têm o elemento Carbono presente em sua estrutura. Os compostos orgânicos estão presentes em todos os organismos vivos, o que faz sua importância ser maior ainda. Com o passar do tempo e com a evolução dos estudos em química orgânica, compostos deste tipo estão cada vez mais presentes no nosso cotidiano, sejam eles roupas, alimentos, plásticos, combustíveis, etc. Além do carbono, os elementos químicos hidrogênio, oxigênio e nitrogênio também são muito presentes em compostos orgânicos.
Algumas características importantes desses compostos são:
• Fazem predominantemente ligações covalente;
• Compostos orgânicos formados somente por carbono e por carbono e hidrogênio são apolares. Quando, na molécula de um composto orgânico, houver um outro elemento químico além de carbono e hidrogênio, suas moléculas passarão a apresentar uma certa polaridade;
• O carbono é um capaz de se ligar a outros carbonos, formando longas cadeias carbônicas;
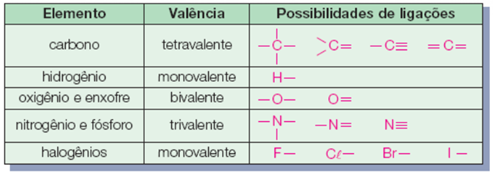
• O carbono é um elemento tetravalente, ou seja, faz 4 ligações. O hidrogênio é monovalente, o oxigênio é bivalente e o nitrogênio é trivalente;
• Dentre as 4 ligações que podem ser feitas pelo carbono, pode-se ter a presença de ligações duplas e/ou triplas.
PSIU!!
Existem compostos com carbono que não são compostos orgânicos, são eles: Os Carbonatos, os Cianetos, o CO e o CO2.
Exemplo:
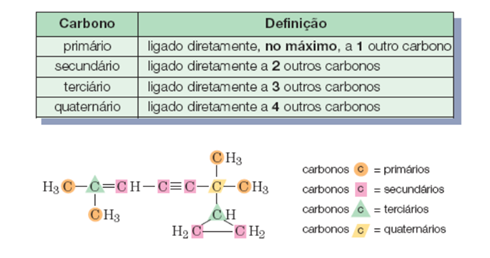
Classificação do carbono
Em uma cadeia carbônica, o carbono pode ser classificado de acordo com o número de outros átomos de carbono a ele ligados.
PSIU!!
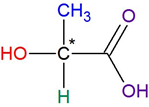
Carbonos assimétricos ou quirais são aqueles que possuem 4 ligações sigma realizadas com 4 ligantes diferentes.
C* = Carbono quiral
Ligações sigma (σ) e pi (π)
Uma outra forma de classificar o carbono é quanto aos tipos de ligações por ele feitas, observe:
Carbono saturado: quando apresenta quatro ligações simples. Essas ligações são denominadas sigma (σ).
Carbono insaturado: quando apresenta pelo menos uma ligação dupla ou tripla. Essas ligações possuem uma ligação denominada pi (π).
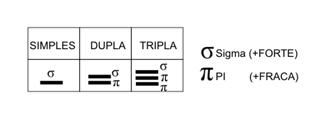
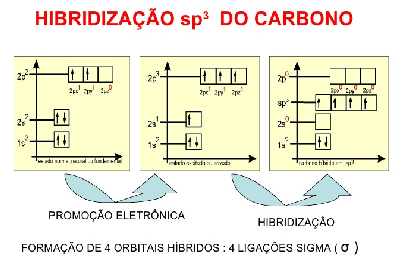
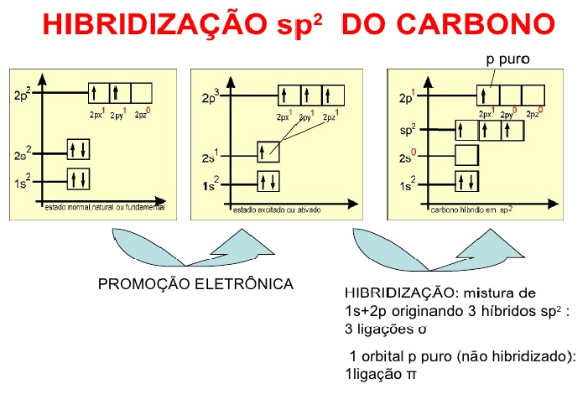
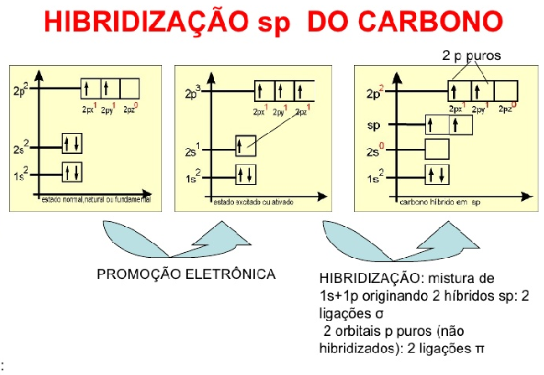
Hibridização
Para realizar quatro ligações do tipo sigma, o carbono deveria apresentar quatro orbitais incompletos, esses orbitais seriam os responsáveis por realizar as ligações sigma. Mas quando paramos para observar os orbitais do carbono, vemos que isso não é possível.
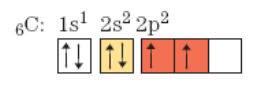
Afim de conseguir adquirir os seus 4 orbitais incompletos para realização das suas 4 ligações sigma, o carbono sofre um processo chamado de hibridização, é assim adquire seus 4 orbitais incompletos, o q o torna um elemento tetravalente.
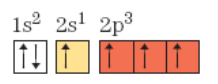
A partir da hibridização, podemos classificar o carbono como tendo hibridização dos tipos sp, sp2 ou sp3.
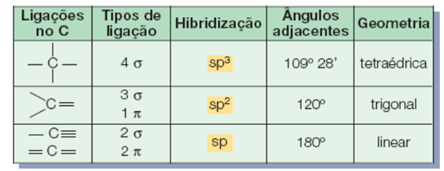
Aprofundando, veremos:
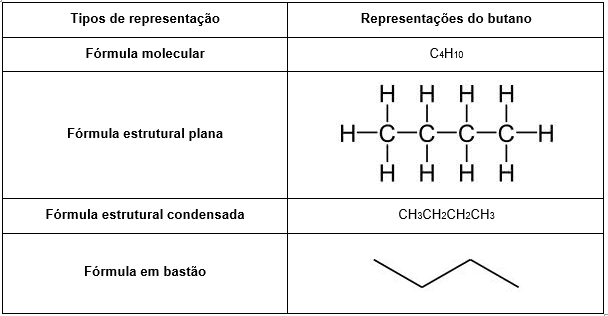
Forma de representação
Existem diferentes formas(fórmulas) de representação para moléculas orgânicas, dentre elas estão:
HIDROCARBONETOS
Hidrocarbonetos são compostos formados por carbono e hidrogênio e constituem uma classe muito numerosa e importante, pois formam o “esqueleto” de todos os demais compostos orgânicos.
Exemplos em nosso cotidiano:

Nomenclatura
De uma forma geral, os hidrocarbonetos seguem uma nomenclatura assim:
Posição dos radicais/ramificações (caso exista) + Prefixo (em relação ao número de carbonos da cadeia principal) + indicativo de ligação (ligação simples, dupla, tripla…) + O (terminação de hidrocarbonetos)
Prefixos
1c -> Met
2c -> Et
3c -> Prop
4c ->But
5c -> Pent
6c -> Hex
7c -> Hept
8c -> Oct
9c -> Non
10c -> Dec
11c -> undec
12c -> dodec
Indicativo de ligações
Ligações simples -> an
Ligações duplas -> en
Ligações triplas -> in
Ligações duas duplas -> dien
Ligações duas triplas -> diin
Alcanos
Os alcanos são considerados hidrocarbonetos de cadeia aberta, saturada de fórmula geral:
CnH2n+2
Nomenclatura
A nomenclatura dos alcanos é denominada com o uso do prefixo correspondente ao número de átomos de carbono, seguindo do sufixo ano, que representa as ligações simples entre os átomos de carbono.
Exemplo:
a)CH4 🡪 Met(1 carbono) + an(somente lig. simples) + o(hidrocarboneto) = Metano
b)CH3 – CH3 🡪 Et(2 carbonos) + an(somente lig. simples) + o(hidrocarboneto) = Etano
c)CH3 – CH2 – CH3 🡪 Prop(3 carbonos) + an(somente lig. simples) + o(hidrocarboneto) = Prop
Alcenos
Alcenos (alquenos, olefinas) são todos os hidrocarbonetos de cadeia aberta, insaturada, podendo assim apresentar uma dupla-ligação entre átomos de carbono, de fórmula geral:
CnH2n
Nomenclatura
Analogamente aos alcanos, na nomenclatura dos alcenos, damos o prefixo correspondente ao número de átomos de carbono, seguido do sufixo eno, que apresenta presença de uma dupla-ligação entre os átomos de carbono.
Exemplo:
H2C = CH2 🡪 Et (2 carbonos) + em (uma lig. dupla) + o (hidrocarboneto) = Eteno
Alcenos podem ter mais de 3 átomos de carbono na cadeia, quando ocorrer essa situação deve ser indicado na posição da dupla, por números, devem-se numerar a cadeia principal da extremidade mais perto da dupla, separando sempre o número de palavras por meio de hífen.
a)H2C = CH – CH3 🡪1 (dupla entre o carbono 1 e 2) + Prop(3 carbonos) + en(uma lig. dupla) + o(hidrocarboneto) = Propeno (não é necessário colocar o número 1, pois é a única posição possível)
b)H2C – CH2 = CH2 – CH3 🡪2(dupla entre o carbono 2 e 3) + But(4 carbonos) + en(uma lig. dupla) + o(hidrocarboneto) = But-2-eno
c)H2C – CH2 – CH2 – CH = CH – CH2 – CH3 🡪3 (dupla entre o carbono 3 e 4) + Hept (7 carbonos) + em (uma lig. dupla) + o(hidrocarboneto) = Hept-3-eno
Alcadienos
Alcadienos (dienos) são hidrocarbonetos de cadeia aberta, insaturados e portadores de duas duplas-ligações, fórmula geral:
CnH2n−2
Nomenclatura
Os alcadienos seguem a regra dos outros hidrocarbonetos e o sufixo dieno, irá indicar a presença das duas duplas ligações.
a)H2C – CH2 = C = CH3 🡪1,2(duplas entre os carbonos 1 e 2 , 2 e 3) + But(4 carbonos) + dien(duas lig. dupla) + o(hidrocarboneto) = But-1,2-dieno
b)H2C – CH = CH – CH = CH – CH2 – CH3 🡪2,4(duplas entre os carbonos 2 e 3 , 4 e 5) + Hept(7 carbonos) + dien(duas lig. dupla) + o(hidrocarboneto) = Hept-2,4-dieno
Alcinos
Alcinos (alquinos) são todos os hidrocarbonetos de cadeia aberta, insaturada, composto por uma tripla-ligação entre 2 átomos de carbono, fórmula geral:
CnH2n−2
Nomenclatura
Os alcinos permanecem com a mesma regra de nomenclatura dos alcenos. O prefixo correspondente ao número de átomos de carbono, seguindo de sufixo ino, que irá indicar a presença da tripla-ligação.
a)HC ≡ CH – CH3 🡪 1(tripla entre o carbono 1 e 2) + Prop(3 carbonos) + in(uma lig. tripla) + o(hidrocarboneto) = Propino (não é necessário colocar o número 1, pois é a única posição possível)
b)H3C – C ≡ C – CH3 🡪 2(tripla entre o carbono 2 e 3) + But(4 carbonos) + in(uma lig. tripla) + o(hidrocarboneto) = But-2-ino
c)H2C – CH2 – CH2 – CH ≡ CH – CH2 – CH3 🡪 3(tripla entre o carbono 3 e 4) + Hept(7 carbonos) + in(uma lig. tripla) + o(hidrocarboneto) = Hept-3-ino]
Obs: Alcadiinos seguem o mesmo padrão dos alcadienos, porém ao invés de duas ligações duplas, serão duas ligações triplas que farão parte do hidrocarboneto.
Exemplo:
H3C – C ≡ C – C ≡ C – CH2 – CH3 🡪 2,4(tripla entre o carbono 2 e 3 , 4 e 5) + Hept(7 carbonos) + diin(duas lig. triplas) + o(hidrocarboneto) = Hept-2,4-diino
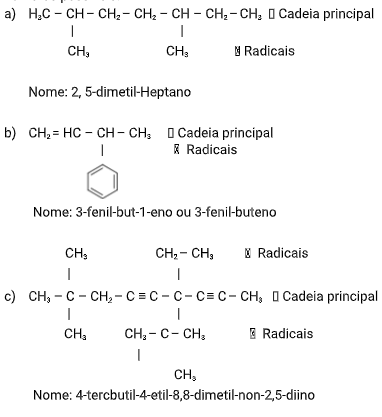
Hidrocarbonetos Ramificados
Após a identificação da cadeia principal, passando obrigatoriamente pelas insaturações (quando existirem) e ainda “sobrarem” partes carbônicas para “fora” da cadeia principal, teremos hidrocarbonetos ramificados. Vamos ver alguns exemplos incluindo os tipos diferentes de hidrocarbonetos já vistos. Observe também, que as ramificações são escritas primeiro e que, se houver mais de uma ramificação, elas devem ser escritas em ordem alfabética, desconsiderando prefixos como di, tri, sec, terc e etc(o prefixo “iso” entra na ordem alfabética). Além disso, os números dos carbonos nas insaturações devem considerar os menores números possíveis: